Roxithromycin
| Chemical Name | : Roxithromycin |
| Category | : Macrolide antibiotics |
| Specification | : EP |
| HS Code | : 29415000.00 |
- Tel: +86-532-83876123
- Fax: +86-532-83876157
- Email: dennis@qingmeibio.com
- Skype: dennis10221
| Structure Formula | : 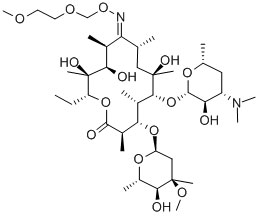 |
| CAS Number | : 56180-94-0 |
| Molecular Formula | : C41H76N2O15 |
| Usage | : The product is a new generation of macrolide antibiotics, mainly for gram positive bacteria, anaerobic bacteria, chlamydia and mycoplasma. The in vitro antibacterial activity of erythromycin and similar, in vivo 1-4 times stronger than that of erythromycin. |
| Items | Standard |
|---|---|
| Appearance | White or almost white crystalline powder |
| Solubility | Very slightly soluble in water, freely soluble in acetone, in alcohol and in methylene chloride. It is slightly soluble in dilute hydrochloric acid. |
| Identification | (1) IR: Conforms to the spectrum of Roxithromycin CRS (2) HPLC: Similar inretention time and size to the principal peak of the reference solution |
| Appearance of solution | (0.2g/20ml methanol) Clear and colourless |
Specific optical rotation | -93°~-96°(Anhydrous substance 0.500g/50ml acetone) |
Impurities A,B,C,D,E,F,H,I,J (For each impruity) | ≤0.5% |
| Impurity G | ≤1.0% |
| Total Impurities | ≤3.0% |
| Heavy Metals | ≤10ppm |
| Water | ≤3.0% |
| Sulphated ash | ≤0.1% |
Assay | 96.0~102.0%(Anhydrous substance) |
| Residual solvents | Methanol≤3000ppm Acetone≤5000ppm Methylene chloride≤600ppm |
We support the below registration services:
1, Argentinian National Institute of Drugs
Instituto Nacional de Medicamentos (INAME)
2, Australian Therapeutic Goods Administration (TGA)
3, Belgian Federal Agency for Medicines and Health Products
Agence Fédérale des Médicaments et des Produits de Santé(AFMPS)
Federaal Agentschap voor Geneesmiddelen enGezondheidsproducten (FAGG)
4, Canadian Health Products and Food Branch Inspectorate(HPFBI)
5, Taiwan Food and Drug Administration (TFDA)
7, Czech State Institute for Drug Control
Státní Ústav pro Kontrolu Léčiv (SÚKL)
8, Czech Institute for State Control of Veterinary Biologicals and Medicines (ISCVBM)
9, Danish Health and Medicines Authority (DHMA)
10, Finnish Medicines Agency (FIMEA)
11, French National Agency for Medicines and Health Products Safety
Agence nationale de sécurité du médicament et des produits de santé (ANSM)
12, French Agency for Food, Environmental & Occupational Health Safety
Agence nationale de sécurité sanitaire de l'alimentation, de l'environnement et du travail (ANSES)
13, German Federal Ministry of Health *
Bundesministerium für Gesundheit (BMG)
14, Icelandic Medicines Agency (IMA)
20, Indonesian National Agency for Drug and Food Control (NADFC)
21, Health Products Regulatory Authority (HPRA)
22, Italian Medicines Agency
Agenzia Italiana del Farmaco (AIFA)
23, Japanese Pharmaceuticals and Medical Devices Agency(PMDA)
24, Korea (Republic of) Ministry of Food and Drug Safety (MFDS)
25, Malaysian National Pharmaceutical Control Bureau (NPCB)
26, Dutch Health Care Inspectorate*
Inspectie voor de Gezondheidszorg (IGZ)
27, New Zealand's Medicines and Medical Devices Safety Authority (Medsafe)
28, Norwegian Medicines Agency (NOMA)
29, Polish Main Pharmaceutical Inspectorate (MPI)
30, Romanian National Agency for Medicines and MedicalDevices (NAMMD)
31, South African Medicines Control Council (MCC)
32, Spanish Agency of Medicines and Medical Devices *
Agencia Española de Medicamentos y Productos Sanitarios(AEMPS)
33, Swedish Medical Products Agency (MPA)
34, United Kingdom's Medicines and Healthcare Products Regulatory Agency (MHRA)
35, United Kingdom's Veterinary Medicine Directorate (VMD)
36, U.S. Food and Drug Administration (US FDA)
37, European Directorate for the Quality of Medicines & HealthCare (EDQM)
38, European Medicines Agency(EMA)
39, World Health Organization(WHO)